
 |
|
Главная страница Влажный воздух [0] [1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] [19] [20] [21] [22] [23] [24] [25] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37] [ 38 ] [39] [40] [41] [42] [43] [44] [45] [46] [47] При р„ <рТ г т Р° (4.52) Формулы (4.51) и (4.52) адекватны формуле (4.49), поэтому выражение (4.50) определяет перепад энтропии при любой температуре воды Гв и окружающей среды Го.с. Таким образом, эксергия воды определяется по формуле бв - Тол \1 о.с -1-1п о.сУ Рп J (4.53) При выводе формулы (4.53) было сделано допущение, что изобары в области воды не отклоняются от линии кипения, т. е. не учитывается величина ев = (кв -кв)- Го.с(sb -sb), (4.54) связанная с изменением энтальпии и энтропии при уменьшении давления воды до давления насыщенного водяного пара при той же температуре. Значения начинают заметно отклоняться от значений h при давлениях, превышающих 230 кПа, а значения - от 5 при больших давлениях. Таким образом, если вода представляет собой взвешенные в воздухе мелкодисперсные капли с радиусом менее 1 мкм (см. табл. 3.14), то расчёт эксергии воды следует производить по формуле (4.47), прибавляя к ней величину . Примеры Пример 4.10. Определить эксергию воды при температуре = 5°С, если температура окружающей среды Го.с = 40°С, а влагосодержание do.c = 0,008 кг вл/кг с.в (р = 100 кПа). Парциальное давление насыщенного водяного пара при температуре воды ts = 5°С определяем по формуле (3.12) 17,504-5 р =0,6112 ехр = 0,872 кПа. 241,2 + 5; Парциальное давление водяного пара в воздухе окружающей среды можно определить из выражения (4.13) р0.с 110-QQQ = 1,397 кПа. " 0,6221 + 0,008 Удельная теплота парообразования г = 2500,64 - 2,369 • 5 = 2488,79 кДж/кг . Эксергия воды, согласно (4.63), ев = 313,15 1,86 278,15 .313,15 + 2488,79 -1-1п 278,15 313,15 j 1 ,278,15 313,15 + 0,46151п 0,872 1,397 = 249,1 кДж/кг. 4.7.4. Эксергия льда Эксергия льда определяется по зависимости бл = ААл-Го.сАул» (4.55) где ДЛд и - разность энтальпий и энтропии между параметрами льда (Гд, Pjj, /1д и Sj) и параметрами водяного пара в окружающей среде (Г, Ро.с о.с Лй- и 5°<). На рис. 4.7 в Г-А-диаграмме показана последовательность процессов перехода из одного состояния в другое: фазовый переход - сублимация 1-2, нагрев водяного пара до температуры окружающей среды 2-3 при Гд < Т или охлаждение водяного пара 2-3 при7д>Г„.,. Энтальпия льда hn~сpTji~fплд • Энтальпия перегретого водяного пара: - при , > Гд hn = CpJn-Гпло + суб + Ср(То.с- Тп), - при Г„., < Гд Ап = СрТл- rwiQ + г суб ~Ср (Гл - Го.с) • Поэтому для обоих случаев А Ал = Ал - Ап = С;,Д7л - Го.с) - Гсуб (4.56) Для определения разности энтропии As„ рассмотрим два варианта, когда Гд > Т и при Гд < Т. ««к**************** 4.7. Эксергия влажного воздуха ******************* 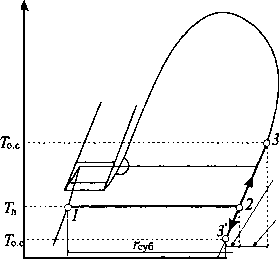 Ср(Тп-То. при Гл>Го.с Сд(То.с- Tjy) при 7;.с> 7!i Яп Лп Рис. 4.7. Соотношение между энтальпиями перегретого водяного пара в окружающей среде и льда Последовательность процессов при Т„ > Т.с представлена на Г-5-диаграмме на рис. 4.8: фазовый переход - сублимация льда 1-2 (перепад энтропии Гсуб/Гд); изотермическое расширение 2-3 до парциального давления водяных паров в атмосферном воздухе (перепад энтропии Rln-); изобарное охлаждение 3-4 до тем- пературы окружающей среды (перепад энтропии минус с п In--). о.с 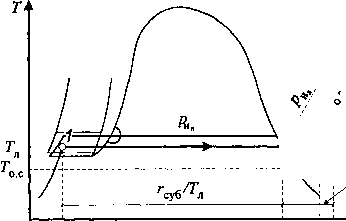 Рис. 4.8. Соотношение между энтропиями перегретого водяного пара I о с f в окружающей среде Йц и льда [0] [1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] [19] [20] [21] [22] [23] [24] [25] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37] [ 38 ] [39] [40] [41] [42] [43] [44] [45] [46] [47] 0.0114 |