
 |
|
Главная страница Принципы преобразования [0] [1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] [19] [20] [21] [22] [23] [24] [25] [26] [27] [28] [29] [30] [31] [32] [33] [ 34 ] [35] [36] [37] [38] [39] [40] [41] [42] [43] [44] [45] [46] энергия ipomoHoe Энергия ipowoHoB \ Изменение "ЧХ, X : сопротивления л Изменение напряжения Энергия (ротонов Изменение напряжения 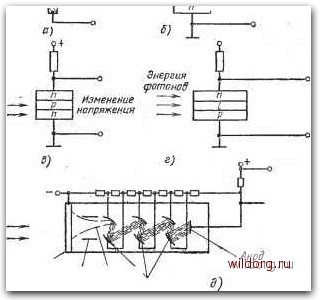 Энергия /ротонов срототтод элетроньЬ фокусируи1ш,ие Диноды пластины , Высоте обратное напряжение сдвига (смещенияУ Изменение напряжения о Энергия
Энергия /ротонов + -о Изменение напряжений Рис. 7.3. Принцип работы преобразователей для измерения потока фотонов: < -слой беспримесного полупроводника; ЯСЯ - прозрачный слой полупроводника о катод, возникающие в процессе фотоэмиссии электроны притягиваются положительно заряженным динодом. При соударении с первым динодом каждый электрон в результате вторичной эмиссии порождает два электрона или более. Таким образом обеспечивается усиление электронов в каждом диноде. . Лавинные фотодиоды реализуют подобный эффект с носителями зарядов в р - п-переходе, который поддерживается при высоком обратном напряжении смещения. Падающие фотоны расщепляют дырочно-электрон-ные носители заряда так, что электроны движутся к п-слою перехода,, а дырки - к р-слою. Высокое напряжение сдвига обеспечивает движение дырок или электронов с такой энергией, которой достаточно, чтобы и далее расщепить пару дырка - электрон и поддерживать лавинный процесс. Фотоэлектрические датчики (рис. 7.3, ж) напоминают основные фотодиоды, в которых р -п-переход используется для обнаружения падающих фотонов. Правда, переход не смещен, а когда он соединяется с нагрузочной схемой, то возникает ток, значение которого зависит от яркости падающего света. Некоторые приборы могут функционировать либо в режиме фотодиода, либо в режиме фотоэлектрического датчика. Тепловые приемники На практике используются три основных типа тепловых приемников: болометрические, пироэлектрические и термоэлектрические преобразователи. Все они выполняют одну и ту же функцию, что и приборы радиационной пирометрии (см. гл. 4), и поэтому подробно не рассматриваются. ГЛАВА 8 ХИМИЧЕСКИЕ ИЗМЕРЕНИЯ Объекты измерений в области химической технологии более, чем в какой-либо другой области, не могут быть детально рассмотрены в этой книге. Объясняется подобное положение тем, что имеется очень много измеряемых величин, которые инженеры включают в число наблюдаемых в химическом производстве. Для всех них •необходимо проектировать и изготавливать соответствующие измерительные преобразователи. Ограничимся рассмотрением наиболее распространенных величин, а именно: кислотности, проводимости и окислительно-восстановительного потенциала. Для их определения требуются соответствующие преобразователи. Химический анализ материалов представляет собой соверщенно иную проблему. Невозможно в этой книге (тем более в одной главе) описать преобразователи, способные измерять уровни веществ в образце, поскольку для этого часто не существует промышленных приборов, и анализ представляет собой более сложный процесс, чем простое измерение. Иногда, правда, определенные типы приборов применяются настолько часто, что становятся типовыми. В качестве примера можно упомянуть сигнализаторы задымления, которые используются в системах противопожарной защиты помещений. Большинство преобразователей, рассматриваемых в этой главе, предназначаются для определения состава образца, отбираемого с помощью различных пробников. Внутри пробника должны обеспечиваться условия для прохождения химической реакции. Кроме того, электрические характеристики пробника, которые подлежат измерению, должны нести информацию об исходном образце. Преобразователи, удовлетворяющие одисанным . требованиям, называются электрометрическими. i Кислотность * Кислотность или щелочность раствора определяется значением водородного потенциала pH=-lo&JH+], где Н"" - концентрация ионов водорода в граммах на литр. Значения рН выражаются числами от О до 14. У чистой воды рН=7, т.е. она является нейтральной - ни кислотной, ни щелочной. Если рН=0, то это чисто кислотный раствор, а если рН = 14, то чисто щелочной. Отсюда следует, что в кислоте концентрация активных ионов водорода больше, чем в щелочи. Электрометрические измерения раствора, при которых определяется его кислотность, обычно осуществля- Н)7 [0] [1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] [19] [20] [21] [22] [23] [24] [25] [26] [27] [28] [29] [30] [31] [32] [33] [ 34 ] [35] [36] [37] [38] [39] [40] [41] [42] [43] [44] [45] [46] 0.0129 |
|||||||||||